От патологоанатомична гледна точка възпалението протича в две основни форми - остра и хронична. Те зависят от персистирането на увреждащия агент, от клиничната симптоматика и от природата (характера) на възпалителния отговор. Острото възпаление представлява бърза реакция, която се развива в рамките на часове, дни, рядко от порядъка на месеци. Независимо от многообразието на факторите, които предизвикват острото възпаление, непосредствената тъканна реакция е стереотипна. Острото възпаление е предимно ексудативно - формира се ексудат, който се излива извън тялото или в телесни кухини, докато хроничното възпаление е предимно пролиферативно - започва размножаване на клетки и различни извънклетъчни елементи, които определят характерната патоморфологична картина.
Зъбни импланти Лицево - челюстна хирургия Адрес на нашата практика Зъболекар
Локално острото възпаление се проявява с нарушения на микроциркулацията, главно на ниво капиляри и посткапилярни венули. Това нарушение се изразява в излив на плазма и плазмени белтъци, включени са и левкоцити. Първоначално се появяват полинуклеарни гранулоцити, последвани от моноцити, лимфоцити, тромбоцити и еритроцити. Стереотипността на реакциите при острото възпаление се определя от освобождаването на химичните медиатори. Те въздействат върху съдовия ендотел, като нарушават интегритета между ендотелните клетки и повишават съдовия пермеабилитет. Медиаторите на възпалението имат хемотаксичен ефект върху левкоцитите. Те обуславят и активация на процеса на фагоцитоза до унищожаването на причинителя. Левкоцитите освобождават също химични агенти, които могат да задълбочат тъканните увреждания. Първоначалните нарушения в участъка на възпалението се съпровождат след това от кръвна стаза и формирането на микротромби.
Реактивните промени, които възникват в тъканите в първите няколко часа след въздействието на увреждащия агент, включват три процеса - промени в съдовия калибър и кръвния ток, повишен пермеабилитет на съдовата стена и формиране на възпалителен ексудат и излизане на левкоцити от съдовете в интерстициалното пространство. Трите процеса се проявяват с излив на ексудат в зоната на тъканното увреждане, който съдържа богата на белтъци оточна течност, фибрин и левкоцити.
Кръвта преминава в микроциркулаторната мрежа от артериолите към широките и тънкостенни венули. Капилярите са свъзващото звено между артериолите и венулите на нивото на микроциркулаторното съдово русло. В прехода към капиляр стената на артериолата има циркулаторен, мощен гладкомускулен слой, играещ ролята на сфинктер. Той регулира протичането на кръвта през самите капиляри. Тяхната стена е тапицирана с непрекъснат ендотелен слой, разположен върху базалната мембрана. В стената липсват гладкомускулни елементи. В много органи (ендокринни и екзокринни жлези, бъбреци, тънкочревната лигавица, чернодробните синусоиди и тези на слезката, костномозъчните синуси) ендотелната тапицировка е фенестрирана, т.е. между клетките има широки отвори. Някои капиляри са по-големи от другите и формират особени канали, през които при нормални условия кръвта протича с предимство. В останалата капилярна мрежа кръвотокът е променлив и се регулира от контракцията и релаксацията на прекапилярните сфинктери. Заради малкия диаметър на капилярния лумен движението на еритроцитите е поединично, в стълб, поради което те често се деформират. В по-широките артериоли и венули ламинарният характер на кръвния ток осигурява централно разположение на кръвните елементи и плазмен, свободен от клетки слой непосредствено до съдовата стена - това се нарича аксиален кръвен ток.
Синус лифтинг Поставяне на зъбни импланти Лицев нерв
При клетъчна и тъканна (органна) активност, например при секрецията на жлезите, абсорбция в чревния епител, мускулно съкращение и други, прекапилярните сфинктери се отпускат, капилярите се отварят и кръвонапълват, за да отговорят на метаболитните потребности на организма. Движението на кръвния ток в артериолите и венулите се регулира от нервни и хуморални механизми, докато в терминалната съдова мрежа (капилярите) локално продуцираните метаболити модулират кръвния ток чрез ефекта си върху прекапилярните сфинктери.
Въздействието на увреждащия агент води до бърза, транзиторна вазоконстрикция на артериолите, която не винаги е възможно да бъде открита при клинични условия - затова и се спори дали изобщо съществува алтеративна фаза на възпалението. Тя се последва от масивна вазодилатация на артериолите и венулите. Наблюдава се отваряне на капилярите и на онези най-малки съдове, които при нормални условия са изключени от общия кръвен ток (резервни капиляри). В резултат на това полседва активна възпалителна хиперемия, като увредената зона силно се кръвоснабдява. Отначало снабдяването с кръв е много бързо, с турбулентен характер, но само след 10 - 15 минути се забавя и се възвръща до нормалното. Фазата на увеличен кръвен ток се последва от неговото намаляване и забавяне. В някои случаи настъпва стаза в съдовете. Причина за последното е нарастналият вискозитет на кръвта в миркоциркулацията поради загуба на плазмена течност от посткапилярните веннули, т.е. настъпва местна хемоконцентрация. Други фактори, които способстват за развитието на стазата, са повишеното тъканно налягане (поради излятата плазма, компресираща съдовата стена) и адхезия на левкоцитите към ендотела, с която се ограничава съдовият лумен.
Повишената съдова проницаемост води до ексудация на плазма и емиграция на клетки - именно това е процесът на формиране на ексудат. Образуването на този ексудат зависи от излива на течност и белтъчни молекули през стената на съдовете на микроциркулацията. При нормални условия дифузията на малки молекули се осъществява чрез концентрационния им градиент - така се осъществява движението през съдовата стена и тъканите и обратно, включително на кислород и въглероден диоксид. За големите молекули дифузията е толкова бавна, че няма практическо значение. Следователно ултрафилтрацията е за сметка на течностите и нискомолекулните разтворими вещества. Още през 1896 година Старлинг доказва че транспортът през съдовата стена е резултат от динамичното равновесие между хидростатичното налягане и колоидо - осмотичното налягане. При нормални условия хидростатичното налягане в артериоларния край на капилярите превишава плазменото осмотично налягане, което е осигурено главно от албумините, при което течностите напускат съда. В същото време с намаляване на хидростатичното налягане и запазване на осмотичното течността отново се увлича обратно в съдовете. Това движение отвътре навън и обратно протича приблизително в еднаква степен, поради което в тъканите течност не се натрупва. При възпаление дилатацията на артериолите се изразява в нарастване и поддържане на високо интраваскуларно хидростатично налягане в микроциркулацията. Течността напуска съдовете по цялата дължина на микроциркулаторната мрежа, със слаба или изобщо липсваща обратна резорбция на излятата течност в тъканите. Въпреки това някои белтъци с по-малка молекулна маса излизат от малките съдове; при нормални условия тяхното количество винаги е минимално, особено при съдове, тапицирани с непрекъснат ендотелен слой. Също така тези молекули при липса на възпаление бързо се връщат в циркулацията чрез лимфната мрежа. Обратно, при наличие на възпаление големи количества плазмени протеини напускат кръвоносните съдове. Осмотичното налягане спада, с което също се затруднява връщането на течността в съдовете. ПРедполага се че излизането на белтъчните молекули се осъществява през ендотелните клетки основно чрез пиноцитозни везикули. Днес вече е доказано че при липса на директно съдово увреждане плазмените протеини напускат съда през междуендотелните пространства на посткапилярните венули. Вазоактивните медиатори въздействат върху ендотелните клетки и причиняват контракция и разширяване на пространствата между тях.
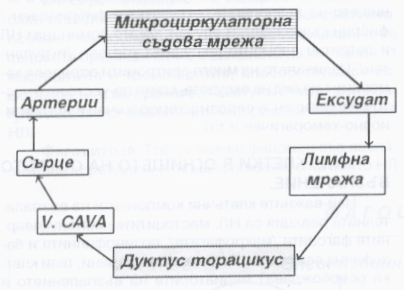
В огнището на възпалението се натрупва богата на белтъци течност - това е така нареченият възпалителен ексудат, който съдържа предимно плазмени белтъци в концентрация около 35 - 50 грама на литър. При контакта си с екстравазалното тъканно пространство коагулационната система се активира и неразтвореният фибриноген в ексудата се превръща във фибрин. Чрез лимфния дренаж на участъка ексудатът бързо се връща отново в микроциркулацията и се поддържа непрекъснат обмен между тъканта и съдовете. Количеството на ексудата в тъканите зависи от техния вид - в компактни, плътни тъкани, фиброзни капсули и други се изливат обикновено малки количества ексудат, които обаче бързо увеличават напрежението и налягането в участъка. При рехави тъкани или в телесни кухини се натрупват големи количества ексудат без особено нарастване на тъканното налягане. Изливът на плазмени белтъци се последва от емиграция на кръвни елементи, които се прибавят към оформящия се ексудат и представляват задължителен негов елемент.

Схема на процеса на формиране и резорбция на възпалителния ексудат. Лимфната система играе основна роля при него - както се вижда, резорбцията на ексудата се осъществява най-вече по хода на лимфните съдове. При това инфекциозните агенти преминават поне през три последователни лимфни възела, където са подложени на допълнителна обработка от страна на имунната система. Клинично това се демонстрира като увеличен и затоплен регионален лимфен възел в зоната на възпалението, но понякога и доста отдалечено - най-вече при по-тежки инфекции, при които имунната система не успява да се справи с локалния инфекциозен процес.
Освен това от съдовете излизат левкоцити и мигрират към посоката на увреждането, което всъщност представлява най-важният момент от формирането на острия възпалителен отговор. Неутрофилните левкоцити мигрират първи, в най-ранния стадий на възпалителната реакция. Преминаването им през съдовата стена се предхожда от подготвителен стадий и протича на няколко етапа - маргинация, селекция на неутрофилните гранулоцити, миграция и хемотаксис. Маргинацията означава че левкоцитите преминават от осевия цилиндър на кръвния ток към периферната част до съдовата стена; следва адхезия към ендотела на посткапилярните венули. Този процес се благоприятства от застоя на кръвния ток в микроциркулаторната мрежа в огнището на възпалението.
В процеса на адхезия основна роля има селекцията на левкоцитите и след това взаимодействието им с ендотелните клетки. Тази селекция се осъществява по рецепторнозависими механизми чрез адхезивните молекули 1 (ELAM 1) и тромбоцитактивиращозависим външен мембранен протеин 140 (GMP - 140). Най-ранната левкоцитна маргинация се осъществява като отговор на експресията на този протеин върху ендотелната клетъчна мембрана. Нормално белтъкът се съхранява в телцата на Weibel - Palade на ендотелните клетки. При стимулация той бързо се транслоцира върху клетъчната мембрана и взаимодейства със съответните рецептори на неутрофилните гранулоцити. В това взаимодействие има известна избирателност - например неутрофилните гранулоцити, отчасти моноцитите и еозинофилните гранулоцити, прилепват главно към стените на възпалените венули, докато лимфоцитите, експресиращи ELAM 1 - до ендотела на венулите в нормалната, отчасти в хронично възпалената лимфна тъкан.
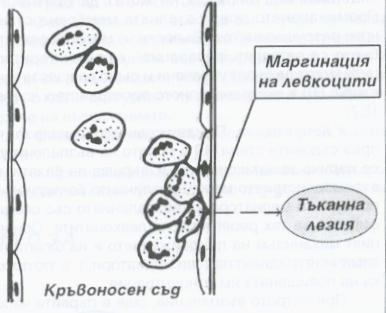
Схема на процеса на маргинация на левкоцитите - те се подреждат покрай стената на кръвоносния съд и се групират по няколко клетки. Обикновено това групиране се случва в участък, който е разположен най-близо до тъканната лезия.
Скоро след това маргинално разположените левкоцити мигрират през стената на венулите и малките вени и отчасти през капилярната стена. Миграцията през съдовата стена се осъществява чрез амебовидни движения. Неутрофилният левкоцит формира псевдоподи, които навлизат между разширените междуендотелни връзки и постепенно увличат цялата клетка. Преди да преминат през базалната мембрана, неутрофилните гранулоцити се разполагат под ендотелните клетки. Самата базална мембрана представлява по-голямо препятствие и поради това левкоцитът може дълго да се задържи под нея без да премине; следва разрушаване на базалната мембрана и клетката излиза извън капилярите. Въпреки че микродефектите бързо се затварят (репарация), единични еритроцити могат да бъдат увлечени и също да излязат в екстравазалното пространство.
Придвижването на излезлите през съдовата стена неутрофилни левкоцити в полето на възпалението се нарича хемотаксис и се извършва на базата на взаимодействието между различните бактериални продукти и медиатори на възпалението със специфичните за тях рецептори на левкоцитите. Основният механизъм на придвижването е на базата на химичния градиент на тези медиатори, т.е. по посока на повишената им концентрация. При острото възпаление още в първите часове на формиране на възпалителната реакция доминиращите клетки са неутрофилните гранулоцити. Те започват да акумулират в полето на възпалението дори още през алтеративната фаза на възпалителния процес. Моноцитите излизат и се натрупват в огнището по-късно, в последните 24 часа от началото на възпалението. При определени агенти са възможни и изключения от тази последователност - например първоначално доминиране на еозинофилни гранулоцити при паразитни инфекции, на лимфоцити при вирусни заболявания, персистиране на неутрофилни левкоцити при някои бактериални инфекции, например стафилококи, и т.н. Най-важните хемотаксични фактори са С5а - фрагментът на комплемента, нискомолекулярните N-формилирани пептиди (N - формил-метионил-левцил-фенилаланин), както и специфични продукти от липидния метаболизъм, включително и левкотриени. Хемотаксични фактори са и продуктите от увредените тъкани - лимфокини, които се секретират от лимфоцитите, както и някои монокини - секреторни продукти на моноцитите и тъканните макрофаги.
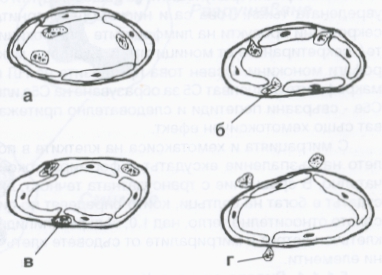
Процес на миграция на левкоцитите извън кръвоносния съд. Това представлява важен физиологичен (а при някои условия - и патофизиологичен) механизъм, по който всеки един жив организъм осъществява своята защита против инфекциозни агенти. Във фаза а) се извършва маргинацията не левкоцитите, описана по-горе; във фаза б) те преминават между ендотелните клетки, във фаза в) е показана пенетрацията на базалната мембрана и във фаза г) левкоцитите са вече извън капилярите - под въздействие на различни хемотаксични фактори те се насочват към мястото на увреждането в тъканите.
С миграцията и хемотаксиса на клетките в полето на възпаление ексудатът е формиран окончателно. В сравнение с трансудатната течност той е богат на белтъци, които определят по-високо относително тегло, съдържа и липиди, клетъчен детрит и мигриралите от съдовете клетъчни елементи. Когато съдържанието на последните е ниско, се говори за серозен ексудат; при излив на по-голямо количество фибриноген в тъканите и активиране на каскадата на кръвосъсирването ексудатът става фибринозен. В случаи, в които доминират неутрофилните гранулоцити и детритни елементи, ексудатът е гноен (пурулентен). При излив на повече еритроцити се говори за хеморагичен характер на ексудата. Чисто хеморагичен ексудат се среща рядко, по-често има смесен характер - серозно - хеморагичен или фибринозно - хеморагичен.
При острото възпаление най-важните клетъчни компоненти са неутрофилните гранулоцити, мастоцитите, еозинофилните и базофилните левкоцити. Когато се стимулират еднократно, тези клетки освобождават медиаторите на възпалението и причиняват задълбочаването на тъканното увреждане. Неутрофилните левкоцити се активират в отговор на фагоцитарни стимули или чрез захващане на хемотаксични медиатори, или чрез прикрепване на антиген - антитяло свързани комплекси към специфични рецептори на техните клетъчни мембрани. Освен това неутрофилните левкоцити имат други рецептори, с които се свързват към FC - веригата на антителата IgG и IgM, с компонентите С5а и С3в на системата на комплемента, с левкотриените и с формираните нискомолекулни хемотаксични пептиди. В резултат на това те осъществяват функциите си в полето на възпалението.
Микроскопски неутрофилните гранулоцити изглеждат като малки клетки, с диаметър от порядъка на 10 микрометра. Предшествениците им от костния мозък попадат в кръвта, където те циркулират само за няколко часа и бързо преминават в лигавиците, където осъществяват основната си функция - антимикробна защита. Те бързо фагоцитират голям брой бактерии и загиват, поради което съзряват ускорено в областта на костния мозък - за период от само 14 дни. В цитоплазмата си съдържат азурофилни гранули - това всъщност са лизозоми, които съдържат неутрални и кисели хидролази - ензими, които предизвикват хидролиза на различни вътре- и извънклетъчни молекули. Под действие на С5а - фактора на комплемента се освобождават ензими от тези гранули, които са водещи при определянето на миркоскопската картина на възпалението както в при нормален, така и при сенсибилизиран организъм. Изключително голяма роля при този процес играят неутралната протеаза, еластазата и колагеназата. От активността на тези ензими зависи дълбочината на увреждането и съответно интензитетът на възпалителната реакция.
Активността на неутралните протеази на неутрофилните левкоцити се инхибира от серумните протеази - L1 - антитрипсин, L2 - макроглобулин и L1 - антихимотрипсин. При дефицит на инхибиторите, който може да е генетично обусловен, резистентността на тъканите срещу увреждането е понижена.
Неутрофилните гранулоцити съдържат в цитоплазмата си и специфични гранули. В тях се откриват главно АФ и бактериални катионни белтъци. Освобождаването, особено на последните, осигурява повишаване на съдовата проницаемост, отделяне на хистамин от мастоцитите и тромбоцитите, способства се хемотаксисът и се проявяват антикоагулантните, коагулантните, пирогенните и антибактериални свойства на неутрофилите.
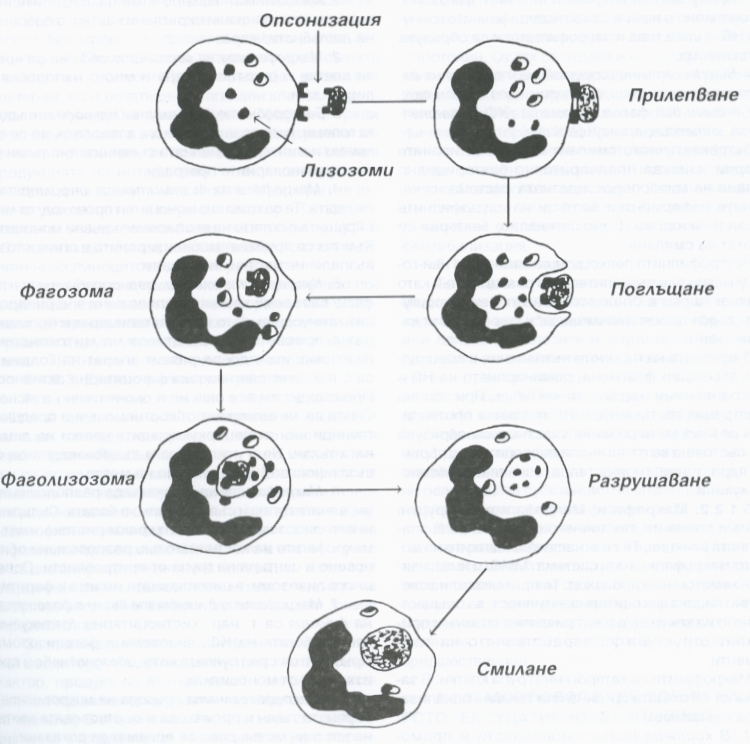
Схема на фагоцитозата - тя е важен елемент на възпалителната реакция, в осъществяването на който неутрофилните гранулоцити играят важна роля. При този процес става поглъщане на бактерии и продукти на тъканния и клетъчен разпад и се осъществява тяхното по-нататъшно смилане. Фагоцитозата далеч не във всички случаи се явява полезен процес за организма - в някои случаи бактериите се натрупват във фагиращите клетки на организма и дори се размножават (например при лепра и гонорея), с което се осигурява прогресиране и хронифициране на възпалението.
Фагоцитозата се осъществява в четири фази, които са показани на горната схема. Първоначално фагоцитът се приближава към микроорганизма или чуждото тяло под действието на хемотаксичните фактори и на системата на комплемента. След това фагоцитът прилепва къмагента, при което важен момент представлява опсонизацията на бактериите и частиците чрез серумните фактори (IgG, термолабилните фактори на С3 - фрагмента на комплемента). Този феномен се съпровожда със силно повишаване на нивото на метаболитните процеси - усилване на аеробната и анаеробната гликолиза и увеличено поглъщане на кислород, така нареченият метаболитен взрив. Той се съпровожда от дегранулация на неутрофилите и отделяне на лизозомални ензими в полето на възпаление. През третата фаза частиците се поглъщат - това става чрез инвагинация на клетката, която впоследствие се затваря и бактерията или друг вреден агент попада във вакуола или така наречената фагозома. Първоначално с нея се сливат специфичните гранули на неутрофилния левкоцит, а след това и азурофилните и се образува фаголизозома. Последният етап е вътреклетъчното смилане на фагоцитираните частици чрез хидролитичните ензими на фаголизозомата - кисела фосфатаза, аминопептидаза, катепсин, арилсулфатаза. Вътреклетъчното смилане на фагоцитираните частици изисква предварителното бактерицидно действие на миелопероксидазната система на катионните неензимни белтъци на азурофилните гранули и лизозима. Единствено загиналите бактерии се подлагат на смилане.
Неутрофилните левкоцити се наричат още микрофаги - те се явяват първи в огнището на възпаление и осигуряват така наречената първа линия на защита. Същевременно те са и клетките с най-голямо участие във възпалителната реакция. В основата на гнойното възпаление и особено при абсцеси и флегмони доминирането им в ексудата е важен морфогенетичен белег. При обилна инфилтрация на тъканта с неутрофилни гранулоцити настъпва протеолитичен разпад в поразения участък и се образува гной, състояща се от загинали левкоцити със сбръчкани ядра. Това са така наречените гнойни телца, изпълващи абсцесните кухини.
Макрофагите са други клетъчни елементи, които са постоянен компонент на възпалителната реакция. Те се отнасят към клетките на моноцитно - макрофагиалната система и имат най-общо хематогенен произход. Те притежават изключително висока фагоцитарна активност, за осъществяването на която съдържат различни ензими и притежават структури за изработването им.
Макрофагите са хетерогенна група клетки. В зависимост от тяхната органна или тъканна локализация се различават монобласти и промоноцити (те се откриват в костния мозък), моноцити (те циркулират в кръвта) и тъканни макрофаги - те са разпръснати из тъканите и са разнородна група клетки. Към тях спадат хистиоцитите на съединителната тъкан, купферовите клетки в черния дроб, алвеоларните фагоцити в белодробния паренхим, фиксираните макрофаги в слезката и лимфните възли, плевралните и перитонеалните макрофаги в серозните кухини, остеокластите в костната тъкан и невроглиалните клетки в нервната тъкан. Макрофагите се разглеждат още като свободни и фиксирани - свободните могат да се придвижват и се появяват във всички тъкани, докато фиксираните са относително постоянни.
Всички различни типове макрофаги имат свои хистологични белези. Така например хистиоцитите са овални или окръглени клетки с бобовидни или вдлъбнати ядра. Макрофагите на серозните обвивки са кръгли клетки с овални ядра и много наподобяват лимфоцити. Белодробните (алвеоларни) макрофаги са доста големи, изпълващи понякога цялата алвеола, но се откриват и в интерстициалната съединителна тъкан на междуалвеоларните прегради. Макрофагите на възпалителния инфилтрат и ексудата са главно с моноцителн произход - от мигриращи в полето на възпаление кръвни моноцити. Към тях се добавят и мобилизираните в огнището на възпалението местни хистиоцити. Купферовите клетки са големи, разположени в чернодробните синусоиди, понякога проминират в лумена им. Богати са на митохондрии, лизозоми, имат добре развит апарат на Голджи и висока фагоцитарна активност. Произходът им не е окончателно изяснен - смята се че възникват от костномозъчни предшественици или от рециркулиращите клетки на лимфната тъкан. Не е изключена и възможността да се възстановяват чрез деление на място.
Макрофагите на слезката са разположени в червената пулпа и съвсем малко в бялата. Съдържат много лизозоми. Подобна характеристика имат и макрофагите на костния мозък, разположени обикновено в центъра на група от еритробласти. Освен голямото количество лизозоми в цитоплазмата им се открива и феритин.
Макрофагите в лимфните възли са с така наречените хистиоцитарни (ретикулни) клетки, богати на кисела фосфатаза, лизозоми и фаголизозоми. Пръснати са сред останалите клетки подобно на звездно небе и произхождат от моноцитите. Микроглиалните клетки произхождат от стволовите клетки на костния мозък и при нормални условия се разполагат в нервната тъкан.
Синовиалните хистиоцити активно се включват при възпалението на ставната обвивка и освобождават лизозомални хидролази, вреждащи подлежащата съединителна тъкан. При това се включват автоимунни механизми и се задлъбочава възпалителният процес - това е особено силно изразено при ревматоидния артрит.
Остеокластите са макрофагите на костната тъкан. Те са много големи, многоядрени клетки, чиято цитоплазма е богата на лизозомални ензими, с помощта на които се осигурява активна фагоцитоза и остеоклазия - разрушаване и резорбция на костната тъкан. Остеокластите се формират от кръвните моноцити чрез сливането им и фиксирайки се в костната тъкан, придобиват специфични особености. С тях се свърза и разрушаването на хрущяла.
Между макрофагите и другите мезенхимни клетки, както и между тях и другите органноспецифични клетки съществуват сложни взаимодействия, поддържащи едно динамично равновесие. Където и да се намират макрофагите (свободни или фиксирани), те проявяват своята висока фагоцитарна и пиноцитозна активност чрез същите механизми, които се наблюдават и при неутрофилните гранулоцити. Те поглъщат и смилат бактерии, но също така и остатъци от загинали клетки, от разрушения междуклетъчен матрикс, фибрин и чужди тела. Макрофагите участват в антивирусната защита на организма, за която голямо значение има продукцията на интерферон. подтискащ вирусната репликация в атакуваните клетки. Макрофагите активно участват и в имунния отговор - по повърхността си те имат рецептори за IgG и С3 - фракцията на системата на комплемента. По този начин те се свързват с антигена, след което поглъщат фиксирания вече антиген в цитоплазмата си чрез пиноцитоза и го разрушават. Макрофагите се появяват малко по-късно в огнището на възпаление в сравнение с неутрофилните гранулоцити и поради това осигуряват втората линия на защита срещу онези бактерии и вируси, с които микрофагите не са в състояние да се справят.
Еозинофилните гранулоцити се откриват значително по-малко в периферната кръв в сравнение с неутрофилите - в рамките на 1 - 3 %. Гранулите им съдържат белтъци, липиди, ензими, особено оксидази и пероксидази. Предшественици в костния мозък са еозинофилните миелоцити. Еозинофилия в кръвта се наблюдава при различни хелминтози, алергични заболявания, медикаментозна алергия и други. Еозинофилните гранулоцити винаги се откриват във възпалителния инфилтрат, като в някои случаи са доминирщата клетъчна популация - при алергичен ринит, бронхиална астма, синдром на Льофлер, алергични васкулити, миокардити, около паразити и т.н. За възникването на еозинофилията има значение един медиатор - еозинофилният хемотаксичен фактор, който се произвежда от базофилните клетки и мастоцитите. Под влияние на различни стимулатори, в това число IgG и системата на комплемента, настъпва дегранулацията на еозинофилите с отделянето на катионни белтъци и пероксидази, които осигуряват основната им функция - фагоцитозата. Освен това тези клетки стимулират повишено образуване на имуноглобулин тип Е от плазмоцитите, с което се включват като ефекторни клетки в огнището на възпаление, особено при алергични реакции. Еозинофилите са в състояние да фагоцитират комплекси антиген - антитяло, еритроцити, бактерии, гъби, могат да убиват и паразити.
Базофилните гранулоцити са най-малочислени - 0.5 - 1 % от всички левкоцити. Диференцират се от клетките - предшественици в костния мозък, като специфичните им гранули се появяват рано в процеса на левкопоеза. Смята се че базофилните левкоцити са предшественици на тъканните баофилни клетки (мастоцитите), които са намират често и в голямо количество в базофилния инфилтрат. Базофилите веднага след действието на увреждащия агент се дегранулират и освобождават едни от най-вазоактивните медиатори на възпалението - хистамин, хепарин и серотонин. От тях се отделя еозинофилният хемотаксичен фактор, активиращият тромбоцитен фактор и бавнореагиращата субстанция на анафилаксията. По повърхността на базофилите има специфични рецептори за имуноглобулин Е. Този тип имуноглобулин се свързва с мембраната на базофила и при въздействие на алерген се стига до масивна дегранулация. Този процес се стимулира допълнително от еозинофилите, особено при състояние на хиперсенсибилизация.
Мастоцитите са едни от основните източници на химични медиатори на възпалението. Разполагат се навсякъде в рехавата съединителна тъкан, перивазално или близко до жлезите и епител на лигавиците. Гранулите им са изпълнени с хистамин, серотонин и хепарин. Цитоплазмата им е богата на кисела фосфатаза, алкална фосфатаза, пероксидази, аденозинтрифосфатаза левцинаминопептидаза и други. На повърхността им, както беше вече описано, са разположени множество рецептори за имуноглобулин Е, при свързването на които с антиген - антитяло комплекси се извършва дегранулация на мастоцитите с всички физиологични и патофизиологични последици от това.
Произходът на мастоцитите все още не е изяснен. Според някои автори това са клетки, които произхождат от базофилните гранулоцити, а според други това са големи лимфоцити. В зрелите, изпълнени с гранули мастоцити, рядко се откриват митози. Вероятно мастоцитите увеличават своя брой не чрез деление, а чрез трансформация на клетки - предшественици.
Морфлогичните форми на острото възпаление са най-общо пет на брой - серозно, фибринозно, гнойно, хеморагично и гангренозно. Серозното възпаление е една от най-често срещаните в клиничната практика форми. При него има серозен характер на ексудата - ниско съдържаните на белтъци, около 25 %, предимно албумин и оскъдно количество клетъчни елементи. Развива се по серозите и лигавиците, но може да се наблюдава и по паренхима на органите.
Трите серозни кухини в организма са плеврата, перикардът и перитонеумът. Те са покрити от серозна обвивка - характерна ципа, която е изградена от мезотел, базална мембрана и съединителнотъканна основа. В тях се натрупва понякога голямо количество течност с леко мътноват вид. Разграничаването на тази течност от трансудата е доста трудно. Серозните повърхности повече или по-малко са помътнени, изгубили са прозрачността си и са хиперемирани. Могат да се видят белтъчни преципитати или съвсем нежни фибринови нишки, отложени по тях. Доста често серозното възпаление е краткотрайно и бързо преминава във фибринозно. При събиране на голямо количество ексудат се притискат органите, в белите дробове се развива ателектаза, а при перикардити се затруднява работния цикъл на сърцето поради компресия на големите венозни съдове, навлизащи в него.
При лигавиците серозното възпаление се среща доста често. Нарича се още катарално възпаление и се предизвиква от вируси, бактерии, химични агенти, бойни отровни вещества и други. Към серозния ексудат се прибавят обикновено слуз и в малко количество епителни клетки. Когато органите със серозно възпаление са в контакт с външната среда, се говори за катарално или серозно - катарално възпаление. Когато към ексудата се прибавят повече левкоцити, възпалението става серозно - гнойно. При наличие на масивна клетъчна десквамация в ексудата се говори за десквамативно възпаление. То обхваща лигавицата на горните дихателни пътища, предимно носа, при хрема, но също така и бронхите, лигавицата на стомашно - чревния тракт и изходните канали на различни жлези. Мукозата е силно набъбнала, зачервена, с разширени и кръвонаълнени капилярни съдове. Ексудатът има слузест, точещ се вид. Серозно - катарален характер има и алергичният ринит (сенна хрема), както и възпалението при бронхиална астма.
В белите дробове огнищната пневмония е най-често със серозен характер, но към серозния ексудат бързо се добавят по-обилно левкоцити и макрофаги и пневмонията става серозно - гнойна. Алвеолите в отделните огнища или сливащи се участъци са изпълнени с ексудатна течност, примесена с неутрофилни левкоцити и макрофаги; такива промени се откриват и в интерстициалната тъкан на белия дроб.
Обикновено изходът от серозното възпалние е пълно възстановяване след резорбция на ексудата. В серозните кухини по изключение ексудатът може да не се резорбира, а да се подложи на организация с формиране на сраствания (шварти) между плевралните листове.
При органите серозна форма на възпаление се среща изключително рядко. Развива се например в кожата след ухапване от пчели, оси, змии, вирусни инфекции (херпес симплекс или вирусът на варицелата), а също и при изгаряния. Между слоевете на епидермиса се натрупва серозен ексудат, който става причина за формиране на везикули или були. Поради това серозното възпаление на кожата се нарича още булозно или везикулозно възпаление. В съединителната тъкан на дермата се формират така наречените кабари, представляващи натрупана серозна течност в долните слоеве, раздалечаваща колагенните и еластични влакна с отлагане и на белтъчна зърнеста материя. В черния дроб серозна течност се натрупва в пространствата на Дисе, най-често в началната фаза на вирусния хепатит или при тиреотоксикоза. В областта на миокарда също при тиреотоксикоза се наблюдава серозен миокардит с наличие на серозен ексудат в интерстициума и единични клетъчни елементи.
В органите серозното възпаление е бързопреходно. Ексудатът се резорбира и възпалението рядко може да приключи с фиброза и склероза.
При фибринозното възпаление в ексудатната течност има повече плазмени белтъци, особено фибриноген, който се превръща във фибрин - от там идва и наименованието на ексудата. Много често фибринозното възпаление се развива по лигавиците и серозите след серозно възпаление. Поради богатството от фибрин по тях се отлагат мембраноподобни или ципести, белезникави налепи (псевдомембрани), които определят и другото название на този ексудат - псевдомембранозен. Отлагането на фибрин винаги се придружава и от процес на некроза на подлежащата тъкан. Според характера на отлаганите псевдомембрани и според дълбочината на некротичните лезии фибринозното възпаление се подразделя на две форми - повърхностна и дълбока. Повърхностната се нарича още крупозна. Среща се в трахеята, белите дробове, червата и серозите. Псевдомембраните са прикрепени слабо към подлежащата тъкан, най-често цилиндричен епител. Отделят се лесно и при падането им се вижда само повърхностна некроза на епитела. Язви не се формират. Такъв характер има възпалението в трахеята при дифтерия, в дихателните пътища при грип, вдишване на бойни отровни вещества или много горещ въздух. Хистологично се установява че епителът на някои места по лигавицата липсва; в останалата част епителът е покрит с дебел слой фибринови нишки.
В областта на лигавиците се оформя налеп от оцветена бледорозова материя, представляваща нишки от фибрин, примесени с левкоцити. Псевдомембраната може да е отдалечена от подлежащата тъкан или да е плътно прикрепена към нея. В лигавицата се открива хиперемия, оток, клетъчна инфилтрация от левкоцити и макрофаги.
В областта на серозните обвивки причината за фибринозното възпаление могат да бъдат микроорганизми - пневмококи, стрептококи и стафилококи; такова възпаление се среща и при уремия, както и стенодопирно при инфаркт на миокарда - епистенокардичен перикардит. Фибриновият налеп се отделя също лесно, поради това че и в този случай е закрепен слабо за мезотела, не навлиза дълбоко и не преминава през базалната мембрана. Вследствие движенията на белия дроб или сърцето фибринът се натрупва неравномерно по плеврите или перикарда на успоредни, изпъкващи ивички или гребенчета. Това дава основание такова сърце да се нарече cor villosum (ресничесто сърце). При обилен ексудат по повърхността се оформя равномерно дебел фибринен налеп.
В белите дробове фибринозно възпаление се наблюдава при класическата крупозна пневмония, която се предизвиква от пневмококи. Промените при нея се развиват в четири стадия, които са описани отдавна. Първият стадий е хиперемичният - при него в алвеолите и интерстициума се излива предимно серозна течност (възпалителен ексудат) с ниско съдържание на фибри. Следва вторият стадий - този на червената хепатизация. При него количеството на фибрина в ексудата нараства и обуславя значително, близко до консистенцията на чернодробния паренхим уплътняване на белодробния паренхим - поради това и стадият се нарича хепатизация. Същевременно в ексудата преминават голямо количество еритроцити и поради това белият дроб освен че е плътен, изглежда и силно зачервен.
Следва третият стадий - при него ексудатът става богат на левкоцити; те стават повече на брой от еритроцитите и поради това белият дроб става със сивкав цвят - стадий на сива хепатизация. Хистологично фибриновият ексудат в алвеолите се вижда под формата на розови, нежни нишки. Те се оцветяват в синьо при реакцията на Вайгерт за фибрин или с РТАН (фосфоволфрамов хематоксилин). През порите на Cohn фибриновите нишки преминават в съседни алвеоли и формират мрежа. Сред нея се виждат разположени първоначално еритроцитите, а след това обилно неутрофилни левкоцити и макрофаги. Левкоцитите инфилтрират и интерстициума, като съдовата хиперемия е силно изразена. В хистологичните препарати фибринът не лежи плътно до алвеоларната стена, а се образува свободна зона между тях, което е артифициално предизвикан от обработката феномен. Възпалението при крупозна пневмония обхваща лоб или цял бял дроб, поради което тя се определя като лобарна пневмония.
Четвъртият стадий се характеризира с резорбцията на ексудата. Протеолитичните ензими, отделяни от разрушените левкоцити, лизират фибрина и поради тази причина ексудатът се резорбира. В други случаи (при малко количество левкоцити) не настъпва резорбция - ексудатът се организира, при което прораства млада съединителна тъкан (гранулационна тъкан). Тя е богата на съдове, узрява и се превръща във фиброзна съединителна тъкан, която изпълва алвеолите. Този процес се нарича карнификация на белите дробове. Консистенцията на органа става плътна, жилава и наподобява месо, откъдето идва и названието на процеса. Функционално се развива прогресираща дихателна недостатъчност. Подобен изход (резорбция или организация) има и фибринозното възпаление при серозните обвивки, където могат да се образуват сраствания между отделните повърхности.
Дълбокото фибринозно възпаление е характерно за дифтерията на фаринкса, поради което и се нарича дифтеритно. Докато повърхностното дифтеритно възпаление се развива в областта на трахеята, където има цилиндричен епител, дълбокото се среща при фаринкса, най-вече върху тонзилите, при ларинкса (и то на истинските гласни връзки), т.е. в места с плоскоепителна тапицировка. Фибриновите нишки на псевдомембраните навлизат дълбоко между и под епителните клетки, поради по-слабите сили на сцепление между тях. Поради това отделянето на мембраните става трудно, със загуба на тъкани и формиране на дълбоки разязвени участъци от лигавицата. Псевдомембраните по тонзилите и ларинкса са плътни, жилави и заедно с възпалителния оток причиняват запушване на горните дихателни пътища и затруднено дишане до задушаване.
Хистологичната картина при острото дълбоко фибринозно възпаление е идентична с тази при повърхностното.
В областта на дебелото черво дълбоко фибринозно възпаление се развива при бактериална дизинтерия. Първоначално измененията стартират като катарално възпаление, което бързо преминава през повърхностно към дълбоко фибринозно. Образуват се масивни, плътни, жълтеникави налепи по чрвената лигавица, при отделянето на които се формират дълбоки некротични зони - дълбоки язви, които понякога дори могат да доведат до перфорация на чревната стена. В стадия на възстановяването на чревната лигавица се формират стриктури, които деформират червото - обикновено по пътя на организацията на ексудата. Подобна картина се наблюдава в дебелото черво при интоксикация със сублимат, а в тънкото - при уремия.
Гнойното възпаление е типът остро възпаление, който се среща най-често в лицево - челюстната област. Тъй като www.maxillofacial-bg.com е проект, насочен основно към лицево - челюстната хирургия, гнойното възпаление ще бъде описано по-подробно тук. Като етиологичен фактор за него най-често се посочва Staphylococcus aureus, но гнойно възпаление може да се предизвика от всякакви коки - стрепто-, гоно-, пневмо-, менингококи, както и от Bacterium pyocarneum, Escherichia coli, тифния бацил и много други. Гнойният ексудат е гъста, полутечна, сивожълтеникава до сивозелена материя. Жълтият цвят се дължи на високото липидно съдържание вследствие разпада на левкоцити - формират се така наречените гнойни телца. Микроскопски в ексудата се откриват много голямо количество неутрофилни гранулоцити; срещат се и белтъци и макрофаги. Нерядко се открива и комбинация от гнойно възпаление с фибринозно и хеморагично.
Органиченото гнойно възпаление се нарича абсцес. Под влияние на протеолитичните ензими, отделени от неутрофилните гранулоцити и бактериите, както и под действието на бактериалните токсини меките тъкани се разрушават (първоначално се размекват), настъпва некроза и се формира кухина. Тази кухина се нарича абсцесна кухина и в нея се съдържа гноен ексудат. Размерите на кухината варират - срещат се малки абсцеси с размер на главичка на топлийка до огромни кухини с диаметър 10 и повече сантиметра.
Възникването на гнойно - абсцедиращия възпалителен процес може да се осъществи по няколко механизма. Възможно е директно внедряване на гноеродната инфекция в тъканите - например около космените фолукули при така наречените фурункули и карбункули. Също така инфекцията прониква по каналикуларен път - през бронхи, жлъчни пътища или пикочопроводи. Така се формират бронхогенни, холангенни, уриногенни и други абсцеси. Понякога бактериите проникват по хематогенен път - хематогенните или пиемичните абсцеси са обикновено множествени, в един или повече органи, със съвсем малки размери и са заградени от хиперемично - хеморагичен вал. В лицево - челюстната област обаче гнойното възпаление се внедрява най-често по съседство - срещат се абсцеси на мозъка при гноен среден отит с остеомиелит на костта, както и абсцеси, обхващащи няколко съседни съединителнотъканни ложи. Хистологично островъзникналият абсцес се представя като недобре ограничен участък, в който тъканта е разрушена и обилно инфилтрирана с неутрофилни левкоцити. По периферията се откриват малко количество макрофаги, чиято цитоплазма е светла и натоварена с липиди.
Хронични абсцеси се срещат по-рядко в клиничната практика. Макроскопски те изглеждат като подутини, рязко ограничени от околната тъкан чрез така наречената пиогенна мембрана. Тя има четири слоя - вътрешен, който е в пряк контакт с абсцесната кухина и се състои основно от неутрофилни левкоцити; вторият слой е изграден от макрофаги, натоварени с липиди - така наречените псевдоксантомни клетки със светла, пенеста цитоплазма и централно или леко ексцентрично разположено ядро. Третият слой се състои основно от лимфоцити и плазмоцити, сред които има обилно количество кръвоносни съдове - това е всъщност гранулационна тъкан. Най-периферно е разположен фиброзен слой (капсула).
Хроничните абсцеси могат да персистират дълго време в костите при хорничен остеомиелит, около апендикса (периапендикуларен абсцес), субфреничен абсцес, в мозъка и други. Ако гнойният ексудат се натрупва в предварително съществуващи или новосформирани кухини, се говори за емпием - например на плеврата, в жлъчния мехур, в маточните тръби и в матката.
Дифузното гнойно възпаление се нарича още флегмон. То се развива в тъкани и органи, в които местните защитни реакции са отслабени, поради което липсва възможност за неговото ограничаване. Флегмонозното възпаление се причинява обикновено от бета - хемолитичния стрептокок от група А. Той продуцира големи количества хиалуронидаза, разграждаща гликопротеините на основното вещество на съединителната тъкан, както и фибринолизин и пептидази, разрушаващи клетъчните структури. Наблюдава се в областта на кожата при еризипел, в меките мозъчни обвивки като гноен лептоменингит, при апендикса като флегмонозен апендицит и в подкожната мастна тъкан (паникулит или целулит). Флегмонозно възпаление е и ангината на Людовик, при която процесът обхваща пода на устната кухина и се разпространява по хода на шийната мускулатура до медиастинума с развитие на гноен медиастинит.
Микроскопски тъканта дифузно се инфилтрира от неутрофилни левкоцити и неограничено се подлага на разпад. Инфилтратът се разпространява по хода на сухожилията, фасциите и интерстициума и разслоява тъканите и органите. Гнойното възпаление протича тежко, с тежки местни и общи прояви. В случай че гнойният ексудат е близо до повърхността на органа, флегмонът може да се усложни с пробив в съответната телесна кухина и да се развие гноен перитонит, плеврит, перикардит или медиастинит. При постепенното прогресиране се оформят изкуствени ходове, наречени фистули. Централната част на фистулния ход е размекната и разрушена, а навън от нея стената е гнойно инфилтрирана. Постепенно ходът може да достигне повърхността и да пробие навън през кожата или в друг орган или кухина.
Флегмонозното възпаление много често ангажира лимфните съдове и лимфните възли, дрениращи съответния участък, с развитие на гноен лимфангит и гноен лимфаденит. В огнището на деструкция възпалението започва да ангажира стените на артериалните и венозните съдове, при което се развива гноен артериит, флебит или тромбофлебит. При ангажирането на съдовете инфекцията може да се генерализира като сепсис или септикопиемия с образуването на множество хематогенни, пръснати в органите и тъканите абсцеси. Развитието на спесиса зависи от редица фактори, но най-вече от реактивността на организма и състоянието на имунната система, главно хуморалния имунитет.
Някои заболявания предразполгат към развитие на гнойно възпаление. Такъв е захарният диабет - той предразполага към развитие на фурункулоза, гноен пиелонефрит и сепсис. Застоят на урината също предразполага към гноен пиелит и пиелонефрит. Застоят на жлъчка пък улеснява развитието на емпием на жлъчния мехур, гнойния холангит и холангио - хепатит. Протрахираният хроничен ход на гнойното възпаление води до обща интоксикация, изтощение и кахексия на организма и нерядко до развитие на амилоидоза.
Гнойното възпаление може да има различен изход. Той зависи от мястото на развитие, от тежестта на промените и възникналите усложения. Абсцесът може да бъде отстранен хирургично (чрез осигуряване на изход за гойния ексудат - при инцизия) или да се отдренира спонтанно - при пробив на повърхността на кожата или в друг орган, тъкан или кухина с формиране на фистулни ходове. Дренираната абсцесна кухина може да се изпълни с гранулационна тъкан, впоследствие заместен от цикатриксиална. При малки абсцеси гнойта може да се резорбира напълно. При благоприятен изход флегмонозното възпаление се подлага на организация, с формиране на цикатрикси или други типове сраствания (шварти), особено при гнойно възпаление на серозните обвивки. Адекватната антибиотична терапия има съществено значение за изхода на гнойното възпаление, както и за предотвратяване на усложненията.
При хеморагичното възпаление в ексудата преобладават еритроцити. Засилена еритродиапедеза настъпва при серозни възпаления, съпроводени с тежки увреждания на съдовата стена. Те са предизвикани от определени инфекциозни агенти - антракс, чума, грипен вирус, вирусите на хеморагичната треска. При антракса мястото на внедряването на инфекцията е най-често кожата.Участъкът се пропива с кървав ексудат и се оформя мехур със синьочервен цвят, откъдето идва и името на заболяването синя пъпка или anthrax (черен). При попадане на бацила през белите дробове се развива тежка хеморагична пневмония. Заболяването може да се прояви и с тежък хеморагичен менингит.
При чумата хеморагичното възпаление се съчетава и с тежки некротични промени в тъканите - кожа, лимфни възли и бели дробове.
При грипа се наблюдават хеморагичен трахеит, бронхит и ринит. При токсичните форми се развиват множество кръвоизливи в органите и тъканите.
Хеморагични възпаления могат да се развият и при различни прояви на хеморагична диатеза, например при авитаминоза С, при петнист тиф, при чернодробни заболявания и други процеси, свързани със синтеза на факторите на съсирване и фибринолиза. В някои случаи туберкулозният бактерий може да причини хеморагично възпаление, както и злокачествените тумори на различни органи поради ерозиране на стените на кръвоносните съдове в участъка на увреждането. Хеморагичният ексудат в серозните кухини у млади хора винаги е подозрителен за туберкулоза, а у възрастните - за карцином.
Гнилостното (путридно) възпаление се причинява от анаеробни микроорганизми като Clostridium perfringens, Escherichia coli, Proteus и други. Те предизвикват масивен гнилостен разпад на тъканите (коликвационна некроза). Подобно на гангрената микробите отделят сероводород, амини, меркаптани, които придават зловонна миризма на ексудата и мръсносивкавозелен цвят на тъканта. Това се дължи на превръщането на хемоглобина в сулфхемоглобин или вердоглобин от сероводорода.
Тъканната некроза се задълбочава и бързо се разширява поради тромбоза, възникваща в съдовете на възпалителното огнище. Към некрозата може да се добави и слаба серозна или хеморагична компонента. При определени микроорганизми в тъканите могат да се образуват големи количества газ, който се натрупва в тъканите и органите под формата на мехури - местен емфизем при газова гангрена. Такива микроорганизми са Clostridium perfringens, Clostridium septicum или hystoliticum. Такава гангрена се формира често като усложнение на тежки пътнотранспортни произшествия, огнестрелни наранявания или големи коремни операции.
Гангренозно възпаление се развива и в белите дробове когато инфекцията попада там от кариозни зъби. Гангрената на белия дроб е тежко заболяване, което много често завършва фатално. Гнилостно възпаление е и номата, която се развива при изтощени деца след прекарани сравнително леки болестни процеси - например морбили.
Гнилостно е възпалението при апендикса - гангренозен апендицит. В случаи, когато липсват периапендикуларни сраствания, гангренозният апендицит се усложнява с тежък дифузен перотонит. Гнилостният разпад на тъканите може да доведе и до самоампутация на апендикса.
Гангренозно възпаление е и ангината на Пол - Винсент. В тонзилите, особено в едната, се развива много тежък, с типичен вид некротичен процес, при сравнително леко увредено общо състояние.
Изходът от острото възпаление може да бъде в няколко насоки. Възможно е ексудатът да се резорбира и да се възстанови първоначалното състояние на тъканта - реституция. Това е най-честият изход от острото възпаление, като в тази ситуация причинителят е напълно ликвидиран. Ексудатът се подлага на резорбция, като първоначално фибринът се лизира от ензимите на неутрофилните левкоцити. Загиналите левкоцити и други клетки, както и продуктите от разпада на тъканите, се поглъщат и смилат от макрофагите. Възможно е хронифициране на възпалението - то настъпва в случаите при които увреждащият фактор персистира и обуславя възникването на хронична възпалителна реакция. Сравнително често се развива и фиброза и склероза - третият възможен изход от острото възпаление. Огнището на увреждане първоначално се замества от гранулационна тъкан, която впоследствие се трансформира в зряла съединителна тъкан. Това е обичайният изход при продължително хронично възпаление. Съединителната тъкан във възпалителното огнище в някои случаи силно се уплътнява и образува цикатрикс; в зоната може да се отложат и калциеви соли и дори да настъпи костна метаплазия (осификация). Този начин на възстановяване на изходната тъкан се нарича субституция. При него възникват повече или по-малко тежки нарушения във функцията на тъканта или органа, тъй като паренхимът не се възстановява и може да настъпи доста сериозна анатомична деформация. Типични примери за това са срастванията в перикардната торбичка и междуплевралните листове след прекаран перикардит (респективно плеврит), който завършва с непълна резорбция на ексудата, последвана от организацията му и разрастване на съединителна тъкан.
Смъртен изход може да настъпи както при острото, така и при хроничното възпаление. Засягането на жизненоважни тъкани и органи от възпалителен процес може да причини тежки увреждания, които понякога са несъвместими с живота. Непълното възстановяване на тъканите и органите може да обуслови тежки функционални нарушения, които също да станат причина за смъртен изход.